1
Campaña
Los biosimilares: “Mucha Vida” para pacientes, sanitarios, administración e industria farmacéutica
BioSim ha puesto en marcha la campaña “Mucha Vida”, una iniciativa de sensibilización que tiene como objetivo destacar la importancia de los medicamentos biosimilares para el acceso a tratamientos de calidad, seguridad y eficacia y la sostenibilidad del sistema sanitario. Con un mensaje optimista, la campaña pone de relieve el impacto positivo de los biosimilares en cuatro áreas fundamentales: los pacientes, que cuentan con más opciones de tratamiento para mejorar su calidad de vida; el sistema sanitario, que optimiza sus recursos y asegura su sostenibilidad; los profesionales sanitarios, que disponen de un mayor abanico de opciones terapéuticas para garantizar la mejor atención a sus pacientes; y la industria farmacéutica, que impulsa la innovación y el desarrollo de nuevas terapias.
Bajo el hashtag #MuchaVida, esta campaña trata de acercar el conocimiento sobre los biosimilares a la sociedad y a los distintos agentes del sector sanitario. Para ello, ya se están llevando a cabo acciones de divulgación, como un vídeo de lanzamiento, una web específica y una mayor presencia en redes sociales.
BioSim
https://www.biosim.es/muchavida/
2
Artículo científico
Evidencia en vida real a largo plazo del tratamiento con un adalimumab biosimilar en pacientes con psoriasis de moderada a severa del Registro de Biológicos e Inmunomoduladores de la Asociación Británica de Dermatólogos (BADBIR)
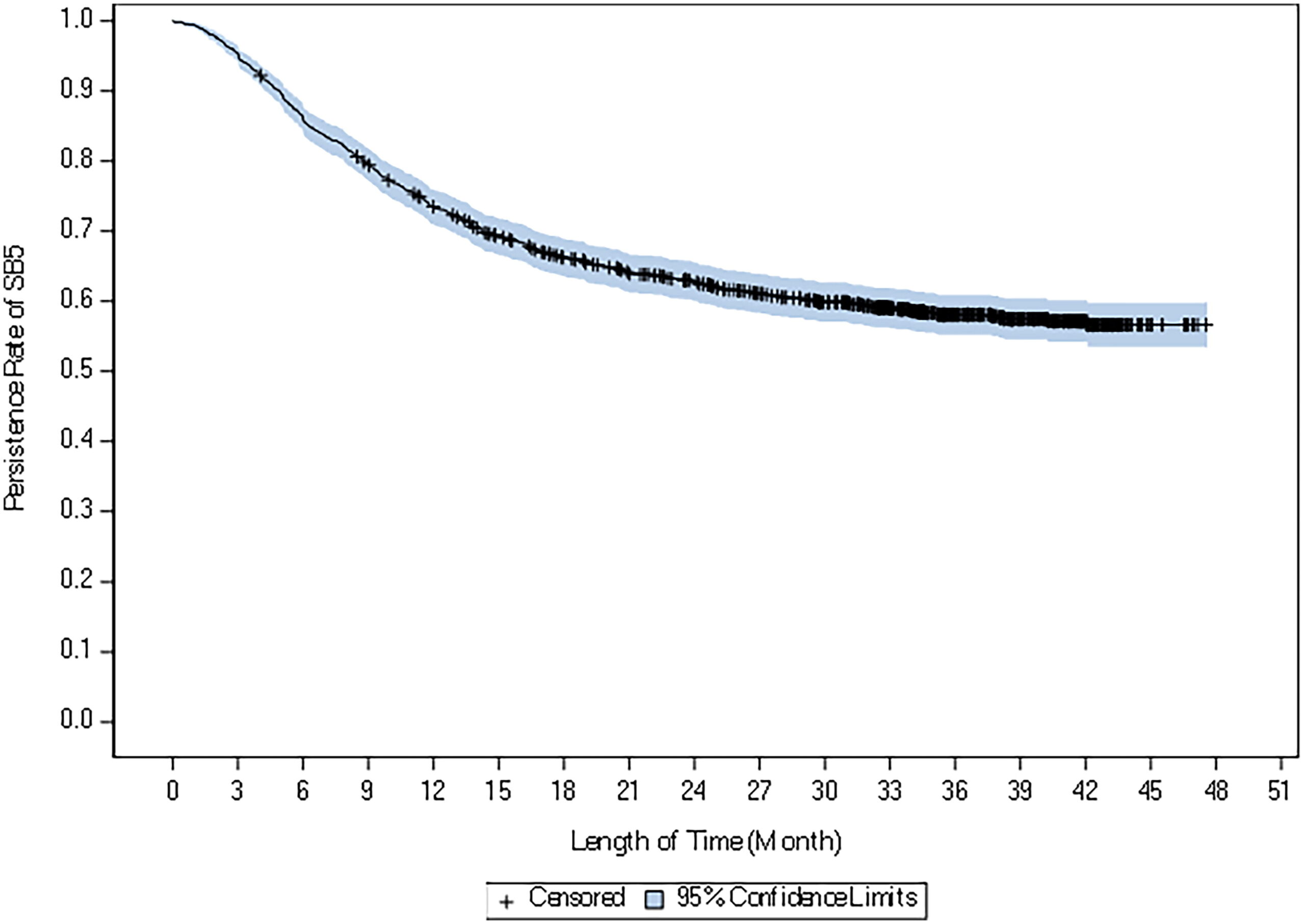 Este estudio prospectivo evaluó la efectividad y seguridad a largo plazo y en vida real de un biosimilar de adalimumab en pacientes con psoriasis de moderada a severa, empleando para ello el registro BADBIR del Reino Unido e Irlanda. Se incluyeron 1195 pacientes tratados entre 2018 y 2022, y se analizó la persistencia del tratamiento como medida de eficacia y tolerabilidad. Los resultados muestran tasas de discontinuación que empiezan en el 26.5% el primer año y ascienden hasta el 43.3% tras cuatro años de tratamiento. Por otro lado, factores como edad, sexo, o índice de masa corporal no afectaron significativamente a la persistencia del fármaco, siendo las principales razones de interrupción la ineficacia y los efectos adversos. Se concluye que la persistencia en la práctica clínica del biosimilar de adalimumab estudiado fue de 2.5 años (mediana), similar a la del adalimumab de referencia, siendo, por tanto, una opción viable para el tratamiento de la psoriasis y permitiendo el acceso potencial de un mayor número de pacientes al tratamiento con un medicamento biológico.
Este estudio prospectivo evaluó la efectividad y seguridad a largo plazo y en vida real de un biosimilar de adalimumab en pacientes con psoriasis de moderada a severa, empleando para ello el registro BADBIR del Reino Unido e Irlanda. Se incluyeron 1195 pacientes tratados entre 2018 y 2022, y se analizó la persistencia del tratamiento como medida de eficacia y tolerabilidad. Los resultados muestran tasas de discontinuación que empiezan en el 26.5% el primer año y ascienden hasta el 43.3% tras cuatro años de tratamiento. Por otro lado, factores como edad, sexo, o índice de masa corporal no afectaron significativamente a la persistencia del fármaco, siendo las principales razones de interrupción la ineficacia y los efectos adversos. Se concluye que la persistencia en la práctica clínica del biosimilar de adalimumab estudiado fue de 2.5 años (mediana), similar a la del adalimumab de referencia, siendo, por tanto, una opción viable para el tratamiento de la psoriasis y permitiendo el acceso potencial de un mayor número de pacientes al tratamiento con un medicamento biológico.
Journal of Dermatological Treatment
https://www.tandfonline.com/doi/full/10.1080/09546634.2024.2434091#abstract
3
Artículo científico
¿Qué papel desempeña la evidencia en vida real en el acceso al mercado de los biosimilares?
El artículo explora el papel de la evidencia en mundo real (RWE, por sus siglas en inglés) en el acceso al mercado de los biosimilares. Se destaca cómo esta evidencia ha respaldado la equivalencia en eficacia y seguridad entre biosimilares y sus productos de referencia, validando aspectos como la extrapolación de indicaciones o la intercambiabilidad. Además, coloca el RWE como piedra angular a la hora de monitorizar el impacto de las políticas de cambio y programas para fomentar la adopción de biosimilares.
Finalmente, se incide en la importancia de aprovechar toda la evidencia que aportan los datos en vida real para demostrar los beneficios asociados a los biosimilares (como ahorros y coste-efectividad), así como para resolver cuestiones relacionadas con las diferentes vías de administración o dosis.
Frontiers in Pharmacology
4
Informe
Alterando el sistema: Una visión general de las prácticas utilizadas por las compañías innovadoras y su impacto en el acceso a medicamentos genéricos y biosimilares
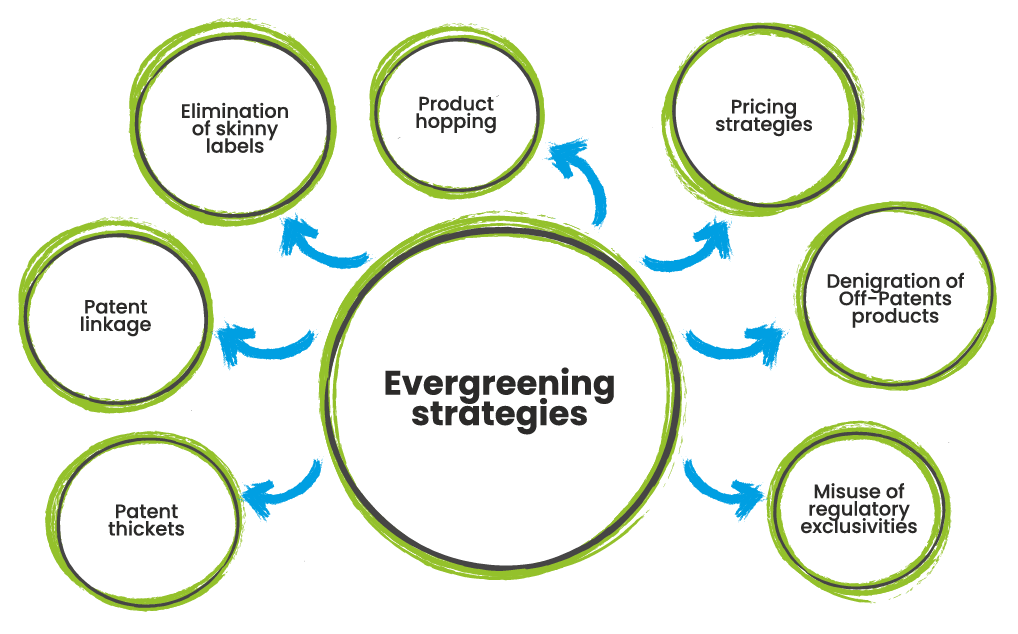
IGBA
https://www.igbamedicines.org/doc/IGBA_IP&Comp_Report-v20250123.pdf
5
Artículo científico
Eficacia y seguridad de un adalimumab biosimilar en pacientes con enfermedad inflamatoria intestinaluso humano en 2024